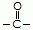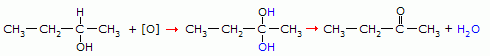Ácidos Carboxílicos
Os ácidos carboxílicos são compostos orgânicos caracterizados pelo grupo carboxila (—COOH), nome e grupo que vem da junção “carbonila (—CO) + hidroxila (OH)”, ou seja, todo ácido carboxílico possui em pelo menos uma das extremidades da cadeia um carbono ligado a um oxigênio e a uma hidroxila . A fórmula estrutural plana da carboxila é:
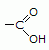
Esses compostos são ácidos fracos, mesmo assim são os compostos orgânicos mais ácidos. Quando têm mais de 10 carbonos, são conhecidos como ácidos graxos. No ser humano, esses ácidos estão presentes no suor, o que faz com que alguns animais reconheçam seus donos apenas pelo cheiro que exalam.
Podem ser obtidos pela oxidação de álcoois ou aldeídos.
Nomenclatura oficial e usual
A nomenclatura oficial é bem parecida com a dos hidrocarbonetos, apenas trocando a terminação para -óico e adicionando a palavra ácido na frente do nome. A numeração é feita começando pelo carbono da carboxila. Exemplo: Ácido etanóico. Outra forma de enumerar os carbonos, é utilizando letras gregas (alfa, beta, gama), contando a partir do carbono vizinho ao carbono da carboxila.
A nomenclatura usual é bastante diversificada, levando em conta o lugar onde são encontrados esses compostos, sendo impossível criar uma regra para ela. Abaixo uma tabela dos nomes usuais, de acordo com o número de carbonos:
1 carbono = ácido fórmico (acido metanóico) (encontrado na formiga)
2 carbonos = ácido acético (ácido etanóico) (vinagre)
3 carbonos = ácido propiônico (ácido propanóico)
4 carbonos = ácido butírico (ácido butanóico) (manteiga rançosa)
5 carbonos = ácido valérico (ácido pentanóico) (extraido da planta Valeriana)
6 carbonos = ácido capróico (ácido hexanóico) (encontrado em caprinos)
2 carbonos = ácido acético (ácido etanóico) (vinagre)
3 carbonos = ácido propiônico (ácido propanóico)
4 carbonos = ácido butírico (ácido butanóico) (manteiga rançosa)
5 carbonos = ácido valérico (ácido pentanóico) (extraido da planta Valeriana)
6 carbonos = ácido capróico (ácido hexanóico) (encontrado em caprinos)
Entre os principais compostos da função dos ácidos carboxílicos utilizados no cotidiano, estão o ácido metanoico, mais conhecido como ácido fórmico, e o ácido etanoico ou ácido acético.
O ácido fórmico é assim chamado porque foi obtido pela primeira vez através da destilação de formigas vermelhas. Esse ácido é o principal responsável pela dor intensa e coceira sentida na picada desse inseto.
O ácido acético é o principal constituinte do vinagre, que é usado em temperos na cozinha, em limpezas e na preparação de perfumes, corantes, seda artificial e acetona.
O ponto de ebulição e de fusão desses ácidos é maior que o dos álcoois, em razão de possuirem pontes de hidrogênio dímeras (entre o oxigênio de ligação dupla, com o OH de outra molécula, e vice versa).
Questão de Enem:
- Sabões são sais de ácidos carboxílicos de cadeia longa utilizados com a finalidade de facilitar, durante processos de lavagem, a remoção de substâncias de baixa solubilidade em água, por exemplo, óleos e gorduras. A figura a seguir representa a estrutura de uma molécula de sabão.
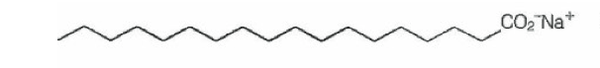
Em solução, os ânions do sabão podem hidrolisar a água e, desse modo, formar o ácido carboxílico correspondente. Por exemplo, para o estearato de sódio, é estabelecido o seguinte equilíbrio:
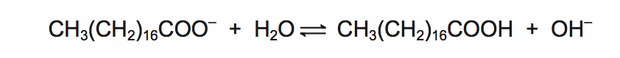
Uma vez que o ácido carboxílico formado é pouco solúvel em água e menos eficiente na remoção de gorduras, o pH do meio deve ser controlado de maneira a evitar que o equilíbrio acima seja deslocado para a direita.
Com base nas informações do texto, é correto concluir que os sabões atuam de maneira:
- Amais eficiente em pH básico.
- Bmais eficiente em pH ácido.
- Cmais eficiente em pH neutro.
- Deficiente em qualquer faixa de pH.
- Emais eficiente em pH ácido ou neutro.